文献解读 | 多组学联用方案用途、优势大总结!南京大学医学院IF 9.4文章应用思路分享~

多组学技术联用,近年来几乎是高分文章,尤其是涉及医学、机制研究的高分文章比较常见的思路框架了。
的确,随着近几年多组学技术的不断更新迭代,层出不穷的新技术不仅丰富了检测对象种类,也提高检测的速度、准确度、覆盖度……在此基础上的多组学联用实验方案,对于提高文章的逻辑性、可靠性和完成度都有非常大的帮助。
但这也造成了一个很多科研工作者,尤其是高分文章发文经验不足的研究者常见困惑:
这么多种技术,我该选什么?

下面,我们就为大家梳理一下几项常见的多组学技术联用方案和对应的研究方向、方案优势:
适用研究方向:疾病机制与生物标志物筛选、病原体-宿主互作、发育生物学与细胞分化
技术联用优势
功能验证:转录组反映基因表达,结合蛋白质组揭示实际功能执行,可验证基因-蛋白表达的一致性或不一致性,识别转录后调控效率,精准锁定靶点,通过数据互补增强结论可靠性。
适用研究方向:疾病机制、药物靶点筛选、代谢调控网络解析
技术联用优势
因果关联:蛋白组反映功能执行层,代谢组反映表型结果层,两者结合构建“调控-表型”网络。
适用研究方向:宿主-微生物互作、疾病标志物筛选、肿瘤微环境、肠道菌群功能研究
技术联用优势
跨物种互作:菌群通过调控宿主转录组(如免疫基因)影响机体。
适用研究方向:信号通路动态调控、疾病分型
技术联用优势
精准动态:修饰蛋白组捕捉翻译后调控,常规蛋白组提供基础表达水平,联合解析明确信号通路。
除了上述介绍的几项外,还有转录组 + 翻译组(Ribo-seq)、微生物组 + 代谢组 + 转录组、scRNA-seq + 空间转录组等适用于不同研究需要的多组学联用方案。
针对客户对于多组学联用方案的偏好,我们精选出几套不同的多组学套餐,助力客户春季科研冲刺:
| 检测项目 | 限时活动价 |
| 16S/18S/ITS 扩增子测序+非靶代谢组学 | 399元/例 |
真核转录组+非靶代谢组学 | 599元/例起 |
| Astral DIA蛋白组 | 559元/例 |
| Astral DIA蛋白组+磷酸化修饰蛋白组 | 1699元/例 |
下面,通过南京大学医学院团队发表的一篇9.4分疾病机制研究文献,来具体分析一下转录组学与蛋白组学联用如何为研究增加亮点~
慢性肾病(CKD)患者肌肉减少症的存在与预后不良有关,尤其是在晚期肾病患者和接受血液透析的肾病患者中常伴随肌肉减少症。为了探索CKD诱导的肌肉减少症的机制,目前的研究集中在骨骼肌的分子改变上。已有一些文章报道过线粒体功能障碍等和其发病机制显著相关,但CKD引起肌肉萎缩的潜在机制尚未得到充分探索。
2025年2月,南京大学医学院附属医院南京金陵医院儿科,在Journal of Cachexia ,Sarcopenia and muscle杂志上发表了题为“Multiomics Analysis Reveals Therapeutic Targets for Chronic Kidney Disease With Sarcopenia”的文章,本文使用饮食诱导的CKD肌肉减少症小鼠模型,基于多组学技术探讨了疾病的发生机制,挖掘潜在的治疗靶点。

小鼠肾脏、血清
转录组学、蛋白质组学
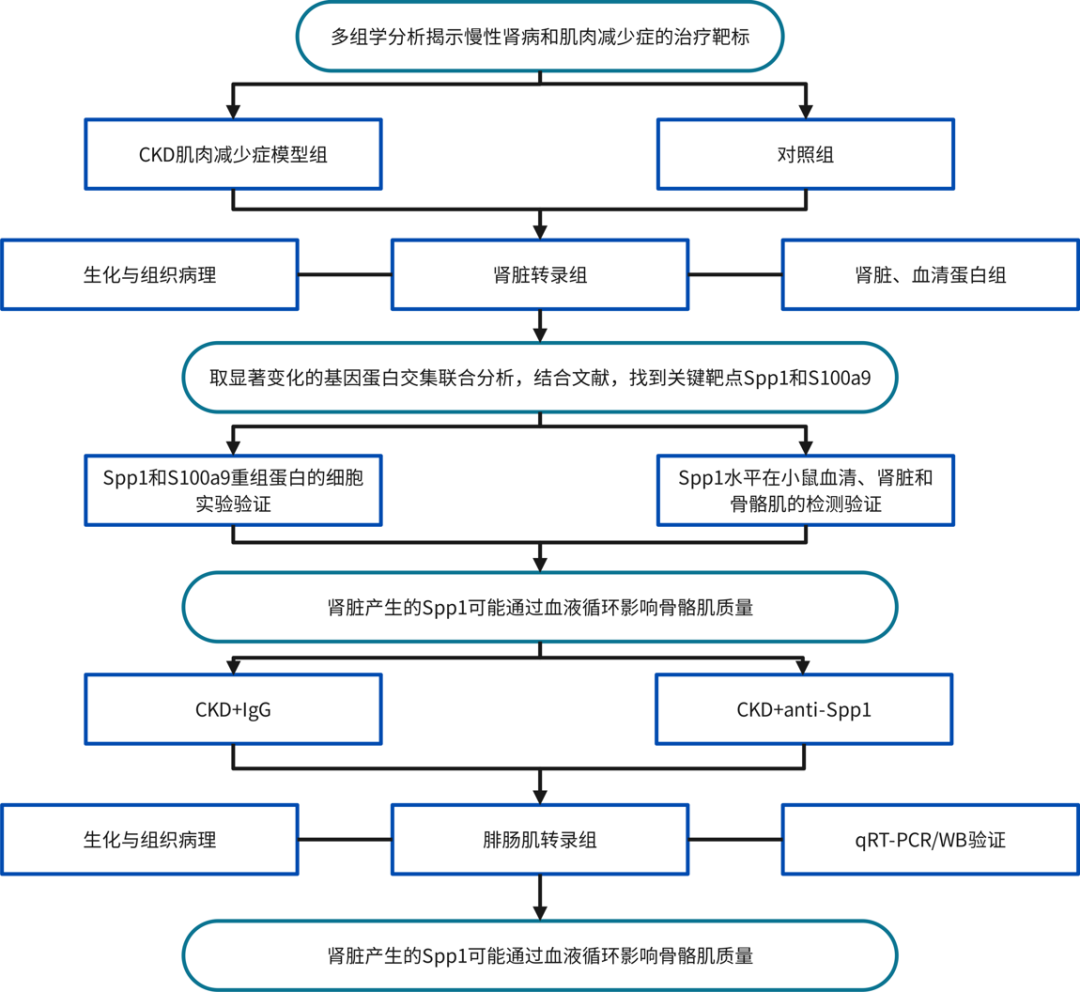
1.建立CKD肌肉减少症小鼠模型
用0.2%腺嘌呤饮食喂养10周龄C57BL/6JNifdc小鼠6周后(图1A),体重和握力逐渐下降,BUN和Scr显着增加(图1B,C)。肾脏病理学分析显示CKD小鼠肾小管萎缩和间质纤维化明显(图1E)。如图1D所示,与NC组相比,CKD小鼠腓肠肌,胫骨前肌和比目鱼肌的重量显着降低。肌肉的病理学和横截面积(CSA)分析表明,CKD小鼠的CSA显着降低(图1F)。结果表明,0.2%腺嘌呤显着降低了小鼠的肾功能并增加了骨骼肌的损失。
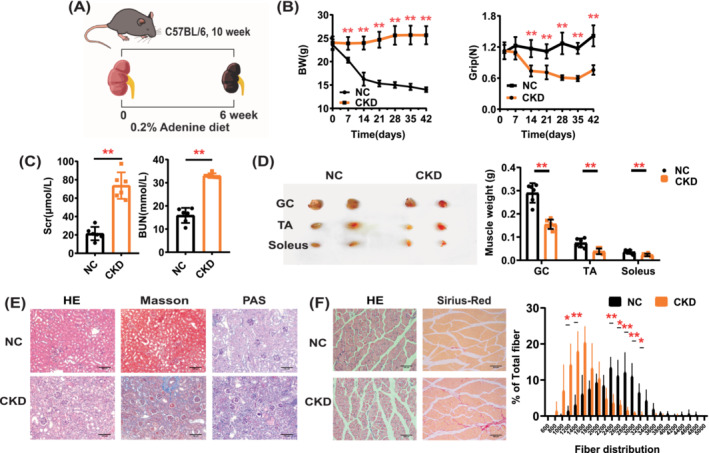
图1 CKD肌肉减少症模型
2.CKD小鼠肾脏转录组和蛋白组及和血清蛋白组分析
基于主成分分析(PCA),肾脏的转录组和TMT以及血清的TMT清楚地分离了CKD和NC小鼠(图2A)。结合来自肾脏转录组和TMT分析的差异表达基因(DEG)/DEP,与对照组相比,CKD组中共有503个基因/蛋白质被共上调,377个蛋白质/基因被共下调(图2B)。随后,共上调和共下调的蛋白质/基因分别与血清TMT的上调和下调蛋白质取交集,NC和CKD组之间肾脏和血清TMT中的29 DEGs/DEPs(图2D,E)。在与图2E中CKD肾脏和血清中表达最多的前10种蛋白质取交集后,鉴定到6种蛋白质,包括Spp1,S100a9,Hp,Orm1,Ltf和Chil3(图2F),为CKD诱导的肌肉减少症提供了潜在的治疗靶点。
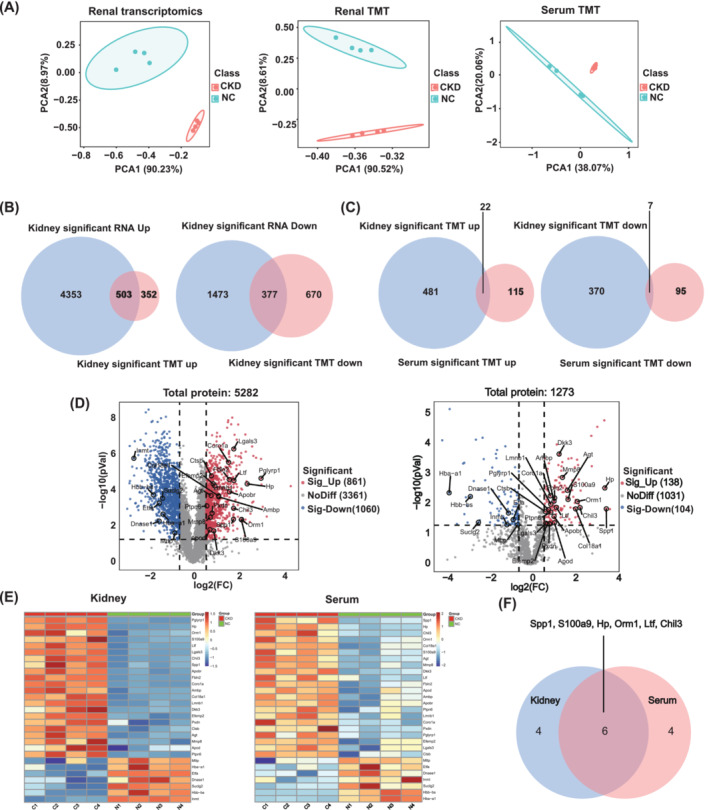
图2 CKD小鼠肾脏转录组和蛋白组及血清转录组分析
3.蛋白组数据揭示CKD小鼠肌肉的分子变化
腓肠肌的TMT蛋白质组学PCA分离CKD和NC小鼠的腓肠肌(图3A)。火山图显示,在CKD和NC小鼠之间检测到2326种蛋白质,其中240种和188种蛋白质分别显着上调和下调(图3B)。热图代表CKD小鼠腓肠肌中上调和下调蛋白中的前30个DEP(图3C)。KEGG途径富集分析表明,包括氧化磷酸化信号传导途径,产热途径,ECM-受体相互作用途径,硫代谢,柠檬酸循环(TCA循环)和血小板活化途径发生了显着改变(图3D)。GSEA显示氧化磷酸化和TCA循环途径显着下调,而ECM-受体相互作用和血小板活化途径显着上调(图3E)。这些结果表明,参与上述途径的蛋白质失调与CKD诱导的肌肉减少症密切相关。
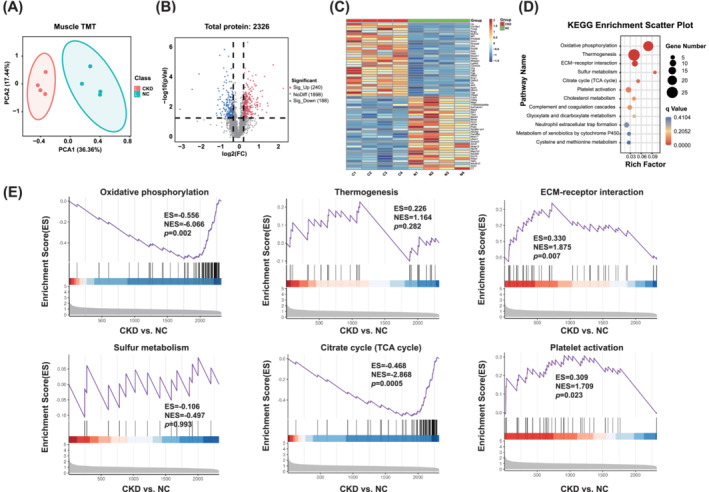
图3 蛋白组学数据揭示CKD小鼠肌肉分子变化
4.肾脏分泌蛋白与骨骼肌最显著改变的KEGG通路的蛋白质之间的相关性
假设肾脏在CKD状态下将特定蛋白质分泌到血液中,并且这些蛋白质可能通过血液循环导致骨骼肌损失。对筛选出的29种蛋白质的表达水平与Scr,BUN,腓肠肌重量和握力之间的相关性进行分析,进一步将图2F中的六种蛋白质缩小到五种:Spp1,S100a9,Hp,Orm1和Ltf。对血清TMT中的这五种蛋白质与肌肉TMT的前六个KEGG途径中涉及的蛋白质进行了相关网络分析,以探索这些蛋白质对肌肉功能的潜在影响。血清TMT中S100a9,Hp,Orm1和Ltf的表达水平与肌肉TMT中氧化磷酸化和产热途径中大多数DEP的变化呈负相关,但与肌肉TMT中ECM-受体相互作用途径中的DEP呈正相关(图4A)。血清TMT中的Spp1,S100a9,Hp,Orm1和Ltf水平与TCA周期中的大多数DEP和肌肉TMT中的血小板活化途径呈正相关(图4A)。血清TMT中的S100a9,Hp,Orm1和Ltf与Selenbp1呈负相关,但与肌肉TMT中硫代谢的Sqor呈正相关(图4A)。这些结果阐明了靶蛋白可能参与的途径。
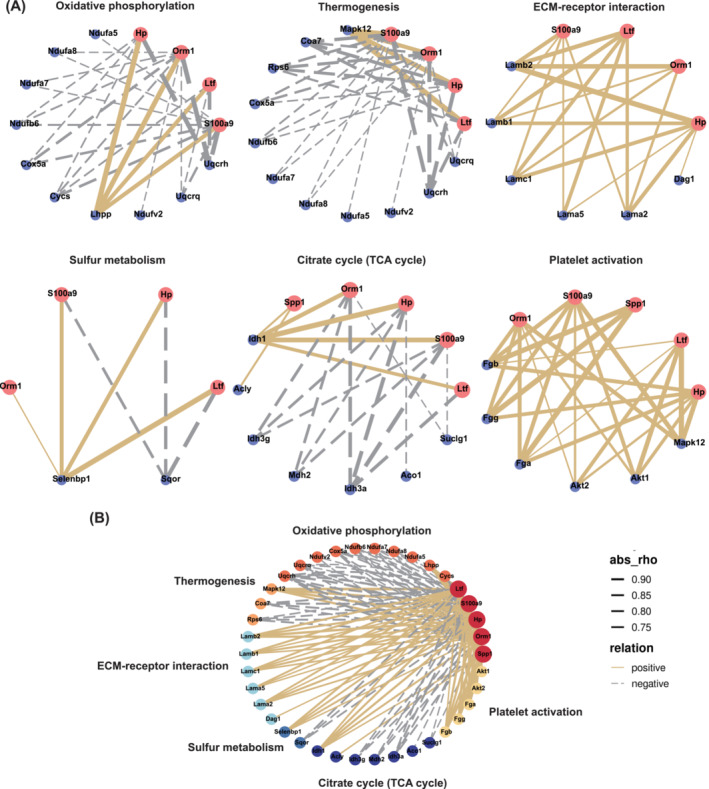
图4 肾脏分泌蛋白与骨骼肌最显著改变的KEGG通路的蛋白质之间的相关性网络图
5.Spp1和S100a9重组蛋白对体外肌管萎缩的影响
经过筛选和文献综述,两种蛋白质Spp1和S100a9成为重点目标用于研究它们对C2C12肌管的影响。图5A显示了细胞实验的流程图。加入S100a9重组蛋白(100 ng/mL)后,atrogin-1的蛋白水平显着增加(图S3A)。然而,加入不同浓度的Spp1重组蛋白后,atrogin-1蛋白水平没有观察到差异(图5B)。分别添加1000 ng/mL Spp1和S100a9重组蛋白后,murf-1蛋白水平显着增加(图5B,图S3A)。免疫荧光染色表明,高浓度的Spp1或S100a9重组蛋白减少了肌管面积(图5C,图S3B)。
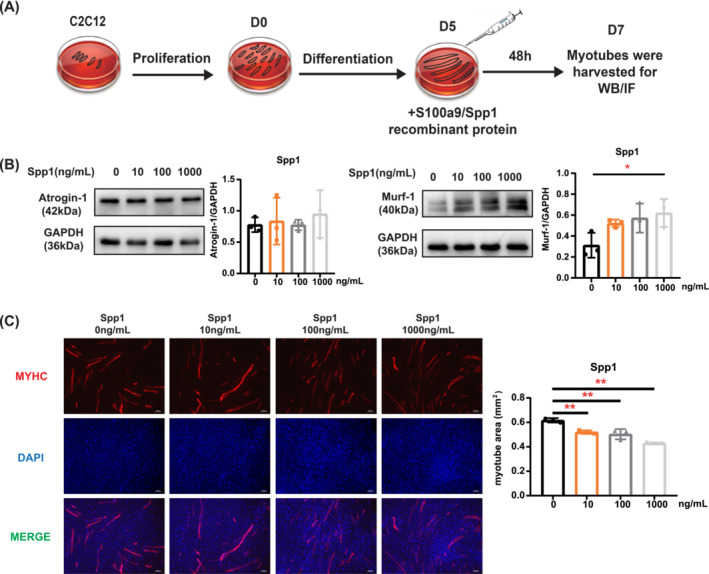
图5 Spp1重组蛋白对体外肌管萎缩的影响
6.CKD小鼠模型肾脏、血清和骨骼肌中Spp1的验证分析
CKD小鼠血清Spp1浓度升高(图6A),这与骨骼肌质量呈负相关(图6A)。qRT-PCR表明,CKD小鼠肾脏中Spp1 mRNA水平显着增加(图6B),WB和免疫组织化学进一步证实了这一点(图6C,D)。同时,免疫组织化学显着增加了CKD患者肾脏中Spp1的表达水平(图6E)。还使用WB检查了骨骼肌中Spp1的表达,发现NC和CKD小鼠之间没有差异(图6C)。因此,肾脏产生的Spp1可能通过血液循环影响骨骼肌质量。
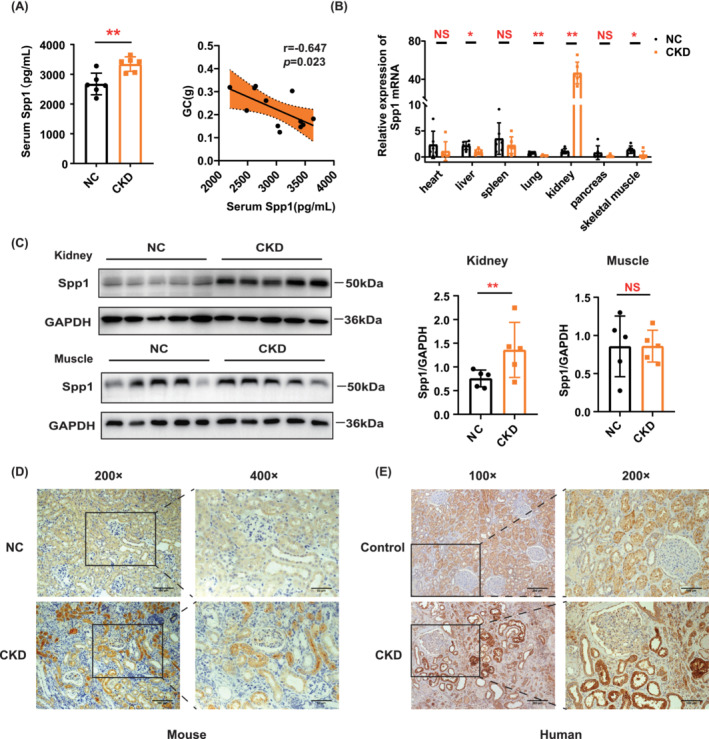
图6 CKD小鼠模型肾脏、血清和骨骼肌中Spp1的验证分析
7.Spp1的药理抑制作用可防止实验性CKD中的肌肉萎缩
在4周的0.2%腺嘌呤饮食后,CKD小鼠每隔一天通过腹膜内注射(100μg/kg)接受一次Spp1中和抗体连续两周(图7A)。用Spp1中和抗体治疗可防止CKD小鼠体重减轻(图7B)。Spp1中和抗体治疗2周后,抗Spp1组的握力显着高于对照IgG组(图7C)。同时抗Spp1组小鼠腓肠肌和胫骨前肌的重量大于对照IgG组(图7D)。循环Spp1的中和降低了CKD小鼠的血液Spp1浓度并轻度改善了血清尿素氮和肌酐水平(图7E)。与对照IgG小鼠相比,腓肠肌CSA的定量显示Spp1中和抗体在终末期时间点右移(图7F)。以上说明Spp1的药理学抑制可防止实验性CKD中的肌肉萎缩。
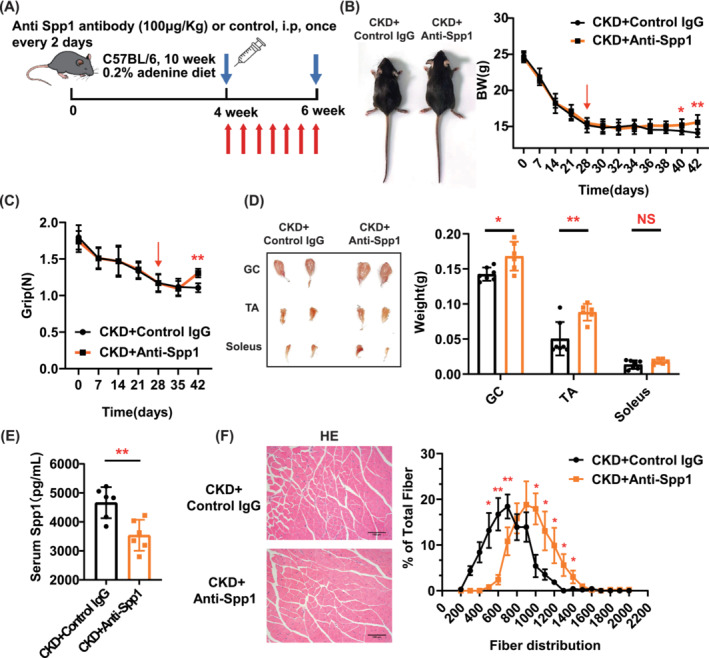
图7 药理学抑制Spp1可预防实验性慢性肾脏病(CKD)中的肌肉消耗
8.转录组鉴定了Spp1药理抑制的骨骼肌萎缩标志物及其验证
为了鉴定CKD小鼠肌肉中受Spp1抑制影响的DEG,作者进行了转录组学分析,比较CKD小鼠中抗Spp1和对照IgG处理的GC肌肉。根据PCA,RNA测序分离了抗Spp1和对照IgG组的腓肠肌(图8A)。火山图显示,在这两组之间检测到25个201个基因,其中1157个和760个基因分别显着上调和下调(图8B)。热图代表了接受Spp1中和抗体治疗后CKD小鼠腓肠肌上调和下调基因中的前30个DEG(图8C)。KEGG途径富集分析表明,这30条途径发生了显着改变,其中蛋白质消化和吸收,胰高血糖素信号通路,apelin信号通路,ECM-受体相互作用和细胞粘附分子的改变最为显着(图8D)。同时验证了用Spp1中和抗体治疗后腓肠肌中骨骼肌萎缩标志物的表达,发现Spp1的药理学抑制在mRNA和蛋白质水平上都改善了肌肉萎缩的标志物(atrogin-1和murf-1)(图8E,F)。这些数据为阻断循环Spp1增加骨骼肌质量的机制提供了线索。
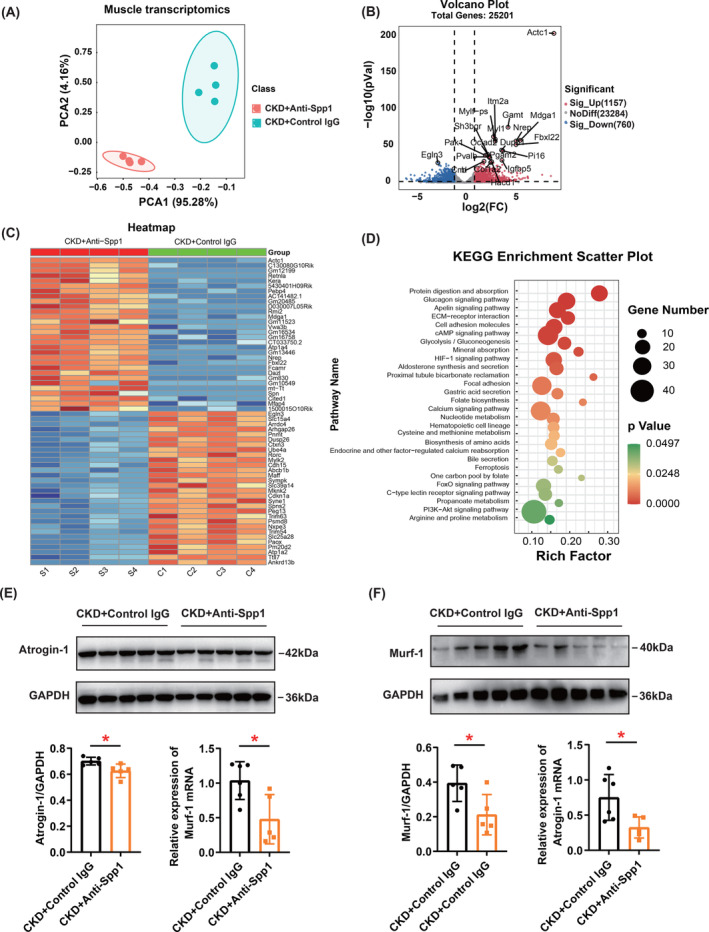
图8 转录组分析鉴定出药理学抑制Spp1后腓肠肌来源的差异表达基因(DEGs),并验证了骨骼肌萎缩标志物
总之,本研究结合了多组学测序,从“肾肌肉”轴的角度探索CKD诱导的肌肉减少症的发病机制。通过多组学分析、细胞评估和动物实验,Spp1可能是治疗肌肉减少症的CKD的有前途的目标。
滑动查看更多:
排版:野凌
审核:三黍生物企宣部




