测序人人做?挖掘才是竞争力!北京林业大学11.7分文章揭秘数据利用关键技巧!

从测序技术诞生至今,短短几十年的飞速发展与普及,造就了现今科研界发文章“人均测序”的现象。
人人都做测序,但对测序结果的开发利用率能达到多少呢?
面对一份测序报告,如果能进一步深入挖掘,拓展出影响因子10分以上的文章完全不是问题。例如下面这篇Science Advances的文章,就是从测序结果出发,利用经典物种杨树,逐步推进,最终拓展为一篇思路严谨、结构完整的优秀文章。

背景:土壤盐碱化对植物生长、作物生产和森林生态系统产生严重有害影响。植物应对盐分压力的能力对于生存和生物质生产至关重要,特别是在多年生树种中。微管细胞骨架在植物应对盐分压力中具有关键功能。皮层微管可以通过快速的微管解聚和重新组装显著影响了盐分压力下植物幼苗的存活率。2025年2日,北京林业大学林金星教授课题组,在Science Advance杂志上发表了题为“Phase separation of the poplar microtubule-associated protein PagPCaP1a aids microtubule depolymerization in response to high salt”的文章,本文表征了来自杂交杨树(Populus alba × P. glandulosa)的微管相关蛋白 PagPCaP1a,并研究了它在植物盐耐受性中的作用。

研究材料:杨树幼苗根系、拟南芥
技术方法:转录组学、遗传转化、RT-PCR、体外相分离
技术路线:
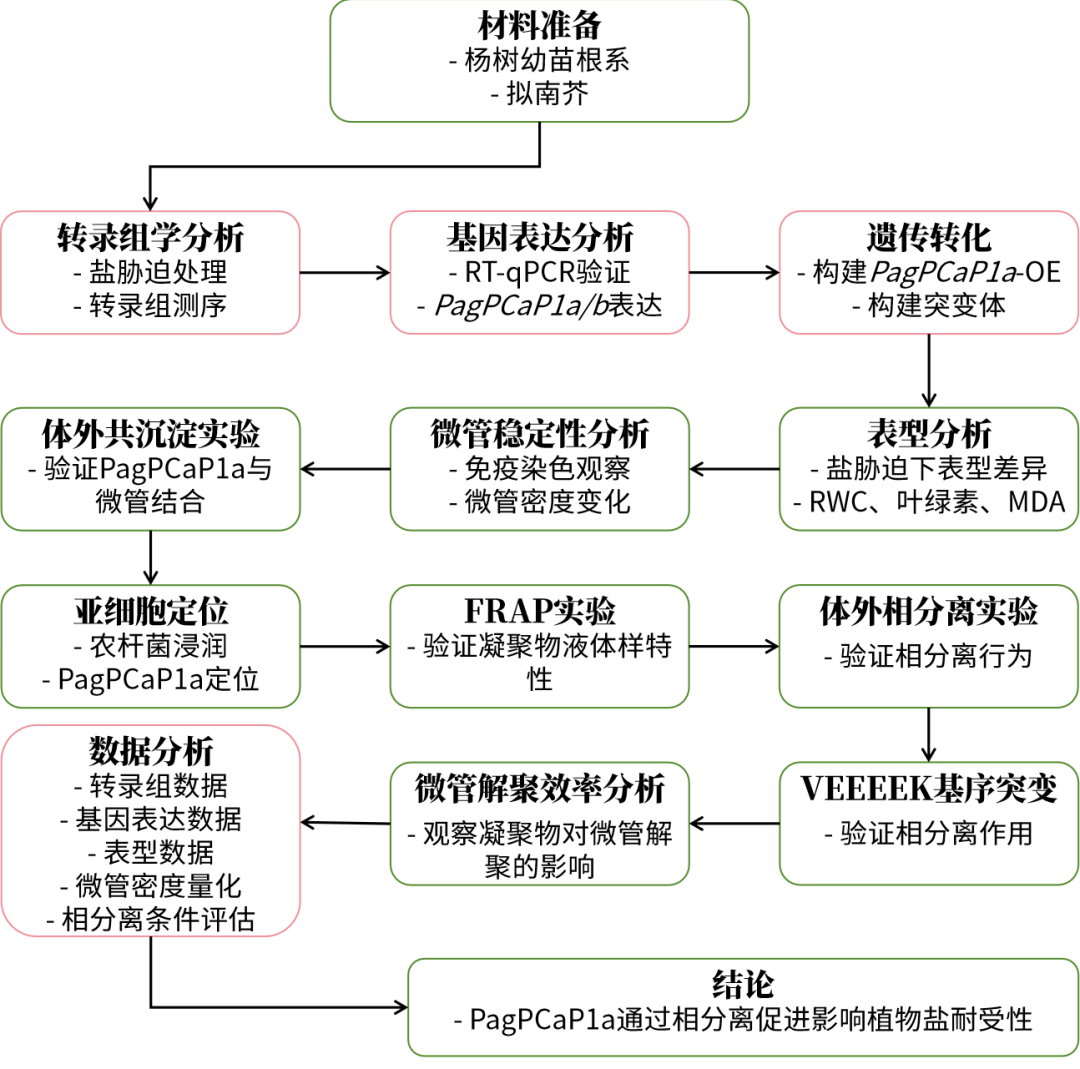
技术路线图
1.PagPCaP1a与杨树的盐胁迫响应密切相关
作者用200 mM NaCl溶液灌溉组织培养生长的植物6小时、12小时、24小时,对照组植物仅用水灌溉,然后收集植物根部进行转录组测序及组间差异分析(图1A、B)。其中最为重要得是GO注释描述为编码质膜锚定蛋白的基因,Potri.003G157100,属于PCaP家族。杨树基因组包含两个PCaP1基因,分别称为PagPCaP1a和PagPCaP1b(图1C)。PagPCaP1a和PagPCaP1b表现出相似的表达模式,在幼叶和茎中显示出一些表达,而在幼根和成熟根中显示出相对较高的表达水平(图1D)。然而,与PagPCaP1a不同的是,PagPCaP1b的表达水平在盐胁迫下基本保持不变甚至略有下降。RT-qPCR分析验证了这一结果(图1E)。以上结果表明,PagPCaP1a可能参与了杨树的盐胁迫响应。

图1 盐胁迫的杨树苗中PagPCaP1b的鉴定和表达分析
2.PagPCaP1b会影响杨树的盐胁迫适应性和微管稳定性
为了评估PagPCaP1a在杨树中的潜在生物学功能,通过遗传转化实验选择了三个PagPCaP1a过表达系(PagPCaP1a-OE)和一个PagPCaP1a基因的突变体。用200 mM NaCl灌溉种植在土壤中的3个月大的WT、Pagpcap1a突变体和OE转基因植物进行为期两周盐胁迫处理,用水作为对照。
PagPCaP1a-OE植物的叶子比WT叶子更萎蔫,而Pagpcap1a突变体植物比WT表现得更好(图2A)。与WT植物相比,PagPCaP1a-OE植物显示出相反的表型,表现出较低的RWC和叶绿素含量以及较高的MDA含量(图2B至D)。同时,在拟南芥的PagPCaP1a转基因互补系(Com#1和Com#2)的存活率低于拟南芥pcap1突变体,恢复到WT(拟南芥品系Col-0)中观察到的水平(图2E和F)。这些发现表明,PagPCaP1a负调控杨树对盐胁迫的响应,其功能在拟南芥中是保守的。
由于PagPCaP1a同源物直接调控微管,为此将15天大的杨树幼苗浸泡在含有200 mM NaCl的液体半强度Murashige和Skoog(MS)培养基中4小时或8小时,使用转移到含NaCl的培养基之前的幼苗作为0小时对照。通过对β-微管蛋白进行免疫染色观察WT、Pagpcap1a和PagPCaP1a-OE#1系中根细胞的皮层微管组织。在暴露于NaCl后,所有基因型的微管密度显著下降(图2G)。特别是,与WT细胞相比,Pagpcap1a细胞中的微管密度下降缓慢,而PagPCaP1a-OE#1细胞中的微管密度下降更快。
为了评估PagPCaP1a对微管的生化功能进行了体外共沉淀实验。从大肠杆菌中生产并纯化了His-PagPCaP1a,并将其与预先形成的Taxol稳定微管一起孵育,His-PagPCaP1a与Taxol稳定微管混合导致大部分PagPCaP1a与微管一起在沉淀中被回收(图2H)。这一结果表明PagPCaP1a直接结合到微管上。另外通过可视化由罗丹明标记的微管蛋白预聚合的微管,单独或在存在PagPCaP1a的情况下,研究了PagPCaP1a对微管动态的影响。显微镜观察表明,与仅观察微管的情况相比,加入His-PagPCaP1a后存在的微管较少(图2,I和J)。这些结果表明,PagPCaP1a作为一个微管不稳定化蛋白,参与了盐胁迫诱导的微管重组。
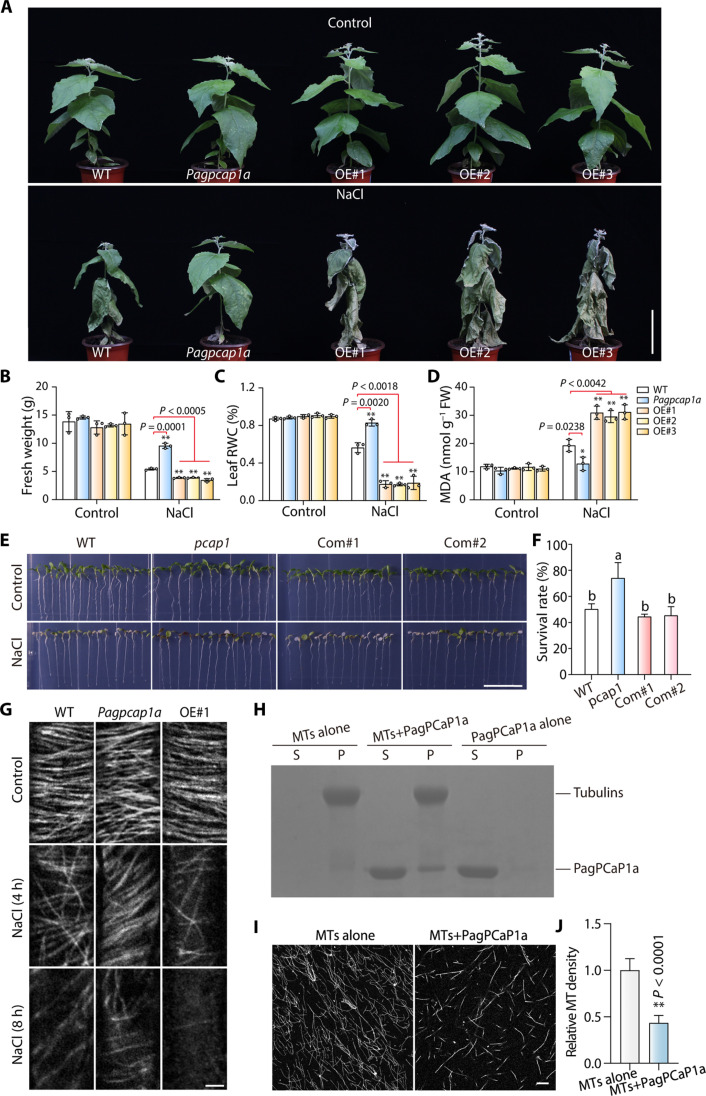
图2 PagPCaP1b会影响杨树的盐胁迫适应性和微管稳定性
3.PagPCaP1a在盐胁迫下在细胞中形成生物分子凝聚物
鉴于PagPCaP1a在盐胁迫响应中的作用,作者评估了PagPCaP1a在正常生长条件下或暴露于盐分压力下的细胞中的亚细胞定位。通过农杆菌介导的浸润将编码PagPCaP1a-mCherry的构建体浸润到烟草(Nicotiana benthamiana)叶中。确定PagPCaP1a-mCherry在盐胁迫下形成诱导的凝聚物,与其在正常条件下的质膜定位相反(图3A)。进一步研究PagPCaP1a在盐胁迫下的杨树中的定位,结果发现,在对照条件下,PagPCaP1a-GFP主要定位在质膜上,并在盐处理10分钟后迅速在细胞质中形成凝聚物(图3B)。
为了确定PagPCaP1a凝聚物是否表现出液体样特性,在杨树原生质体中的PagPCaP1a-GFP凝聚物上进行了光漂白后荧光恢复(FRAP)实验。在实验后,PagPCaP1a-GFP迅速从未漂白区域重新分布到漂白区域(图3,C和D),这表明这些凝聚物具有液体样状态。此外,PagPCaP1a-GFP在转基因拟南芥proAtPCaP1:PagPCaP1a-GFP/pcap1互补幼苗的根细胞中暴露于盐处理后迅速在细胞质中形成凝聚物(图3,E和F),这些凝聚物在FRAP分析下也表现出类似的液体样特性(图3,G和H)。总之,这些观察表明,PagPCaP1a蛋白在响应盐胁迫时在体内形成具有液体样特性的凝聚物。这些数据表明,PagPCaP1a蛋白可以形成动态的凝聚物,这种行为可能与液-液相分离(LLPS)有关。
为了确定盐诱导的PagPCaP1a凝聚物形成是否依赖于Ca2+,在将proAtPCaP1:PagPCaP1a-GFP/pcap1转基因幼苗暴露于200 mM NaCl之前,先用300 μM BAPTA-AM(一种可透过细胞的Ca2+螯合剂)预处理30分钟,单独或在存在BAPTA-AM的情况下暴露于NaCl。暴露于盐胁迫后,BAPTA-AM大大损害了PagPCaP1a凝聚物的形成(图3,I和J)。类似地,钙通道阻断剂LaCl3抑制了根细胞中PagPCaP1a凝聚物的形成(图3,K和L)。这些结果表明,盐诱导的[Ca2+]cyt升高在体内PagPCaP1a凝聚物的形成中起着关键作用。
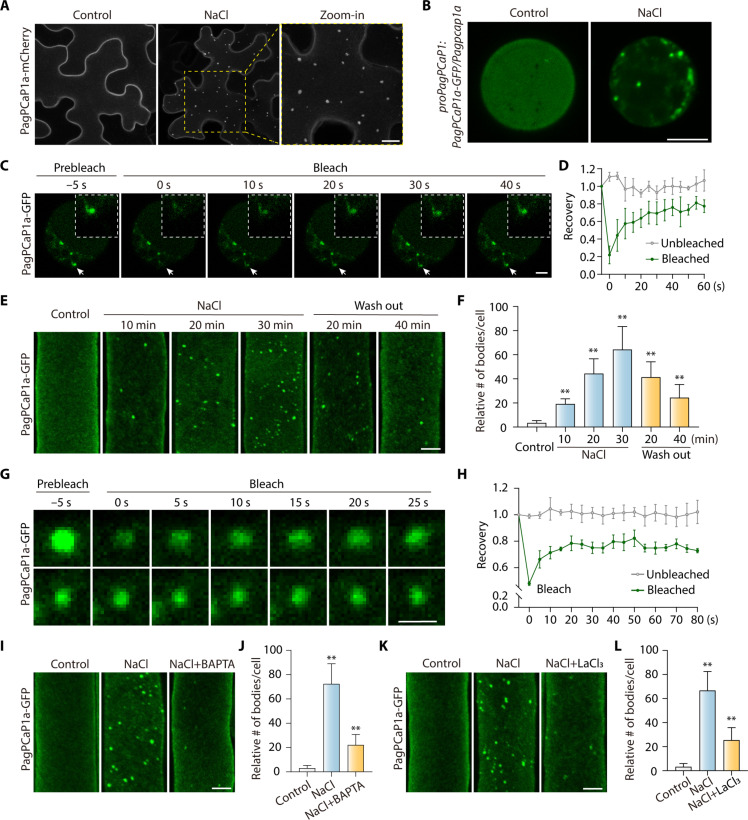
图3 PagPCaP1a响应盐度胁迫而经历可逆和动态凝聚
4.PagPCaP1a在体外进行LLPS
内在无序区域(IDRs)在进行LLPS的蛋白质中很常见,介导生物分子凝聚物的形成。生物信息学分析表明,PagPCaP1a很可能含有IDRs(图4A)。在室温下在有或没有NaCl的情况下孵育纯化的重组PagPCaP1a-GFP,没有任何样本显示出蛋白质溶液的浊度。在反应中加入了CaCl2形式的Ca2+产生了指示LLPS的浊溶液(图4B)。为了确认Ca2+在PagPCaP1a相分离中的作用,在存在NaCl或CaCl2的情况下进行沉淀实验,通过离心分离可溶部分和凝聚相(沉淀),随后进行SDS-PAGE和考马斯亮蓝染色,确定了加入Ca2+促进了PagPCaP1a-GFP凝聚相(沉淀)的形成(图4C)。对浊溶液的显微镜观察显示,PagPCaP1a-GFP/-mCherry形成微米级的凝聚物(图4D)。
体外相分离实验通过系统地改变Ca2+和重组PagPCaP1a-GFP的浓度来生成相图,以评估促进凝聚物形成的条件(图4E)。随着Ca2+(0到10 mM)或蛋白质(5到150 μM)浓度的增加,形成的凝聚物更大且数量更多(图4,F到H)。使用时间序列显微镜观察到单个PagPCaP1a凝聚物的融合,形成了更大和更球形的蛋白质体(图4I)。FRAP实验显示,漂白后的PagPCaP1a-GFP凝聚物的荧光信号在90秒内恢复到接近光漂白前的值(图4,J和K)。这些结果表明,PagPCaP1a-GFP凝聚物具有LLPS所必需的动态特性。
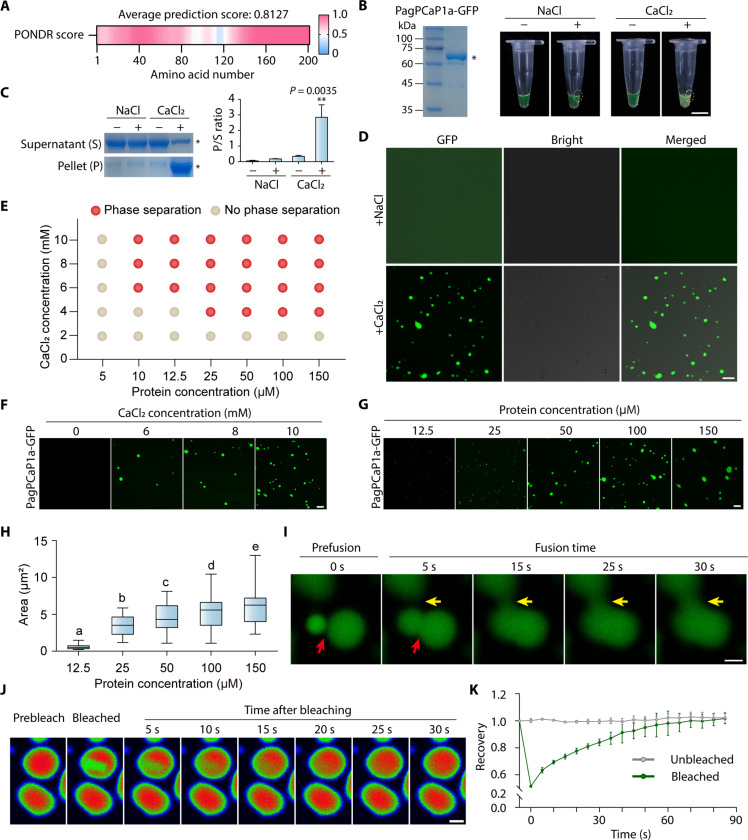
图4 PagPCaP1a在体外进行LLPS
5.PagPCaP1a通过其VEEEKK基序部分以依赖Ca2+的方式进行LLPS
VEExK基序是一个潜在的Ca2+结合位点,并且对拟南芥中Ca2+介导的PCaP1功能至关重要。作者突变了VEEEKK基序中的三个氨基酸,创建了mPagPCaP1a变体(图5A)。在体内的相分离实验中,将PagPCaP1a-mCherry或mPagPCaP1a-mCherry构建体浸润到N. benthamiana细胞中,发现PagPCaP1a-mCherry和mPagPCaP1a-mCherry在对照条件下均定位在质膜上。然而,在暴露于盐胁迫时,PagPCaP1a-mCherry形成了可见的凝聚物,而mPagPCaP1a-mCherry则没有(图5B)。进一步通过在Pagpcap1a突变体杨树获得的原生质体中瞬时表达proPagPCaP1:mPagPCaP1a-GFP或proPagPCaP1:mPagPCaP1a-mCherry来确认这些结果(图5C)。
此外,将proAtPCaP1:mPagPCaP1a-GFP转基因引入到拟南芥pcap1突变体背景中(指定为mCom#1和mCom#2)。在mCom#1和mCom#2幼苗的根细胞中,即使在盐处理条件下,mPagPCaP1a-GFP仍保持其质膜定位(图5D),这与在杨树细胞中的观察结果一致。此外,proAtPCaP1:mPagPCaP1a-GFP无法补偿拟南芥pcap1突变体在盐分压力下更高存活率的表型(图5,E和F)。这些发现揭示了依赖Ca2+的相分离对于PagPCaP1a蛋白在幼苗响应盐分压力时的功能至关重要。
为了研究VEEEKK基序在PagPCaP1a相分离中的重要作用,作者检测了mPagPCaP1a在体外的相分离。在相同浓度的Ca2+存在下,mPagPCaP1a的浊度与PagPCaP1a相比显著降低(图5,G和H)。对溶液的显微镜观察显示,mPagPCaP1a只能形成散乱的、不规则形状的聚集体,因此其相分离能力大大降低(图5,I至K),证实了Ca2+对PagPCaP1a相分离的重要作用。
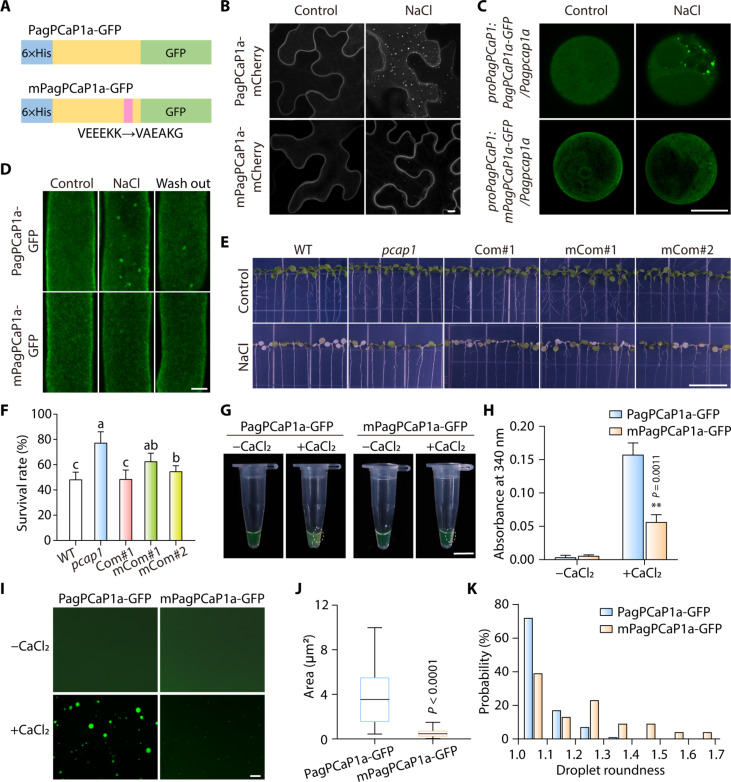
图5 VEEEKK基序对Ca2+介导的PagPCaP1a相分离至关重要
6.PagPCaP1a凝聚物在盐胁迫下增强微管解聚的效率
由于PagPCaP1a在盐胁迫下使微管不稳定并形成蛋白质凝聚物,因此作者研究了PagPCaP1a凝聚物存在下微管的行为。PagPCaP1a-mCherry和MBD-GFP在本氏烟草细胞中瞬时共表达。共聚焦显微镜显示,当细胞暴露于200 mM NaCl时,大多数PagPCaP1a-mCherry凝聚物与微管共定位(图6A)。为了证实这些结果,进一步培养了共表达PagPCaP1a-GFP和mCherry微管蛋白的转基因拟南芥植物。在这些植物中,PagPCaP1a-GFP凝聚物与mCherry微管蛋白标记的皮质微管共定位,特别是在用NaCl处理的细胞中(图6B)。因此,PagPCaP1a凝聚物在盐胁迫下定位于微管。
接下来,研究了PagPCaP1a凝聚物对微管组织的影响,方法是使用由罗丹明标记的微管蛋白聚合的微管,并将其与重组纯化的His-PagPCaP1a或His-mPagPCaP1a一起孵育。在没有Ca2+的情况下,与对照相比,PagPCaP1a或mPagPCaP1a的存在下微管的密度降低,PagPCaP1a和mPagPCaP1a之间没有显著差异。在Ca2+存在的情况下,PagPCaP1a存在下的微管密度显著低于mPagPCaP1a存在下的微管密度(图6C)。微管密度的量化表明,PagPCaP1a凝聚物在Ca2+存在下可以加速微管解聚约两倍,与没有Ca2+且没有相分离的条件相比(图6D),这表明PagPCaP1a的LLPS加速了微管解聚。总之,这些结果表明,盐分压力诱导PagPCaP1a的LLPS,这些凝聚物定位到微管上以促进其解聚,从而影响植物的盐耐受性。
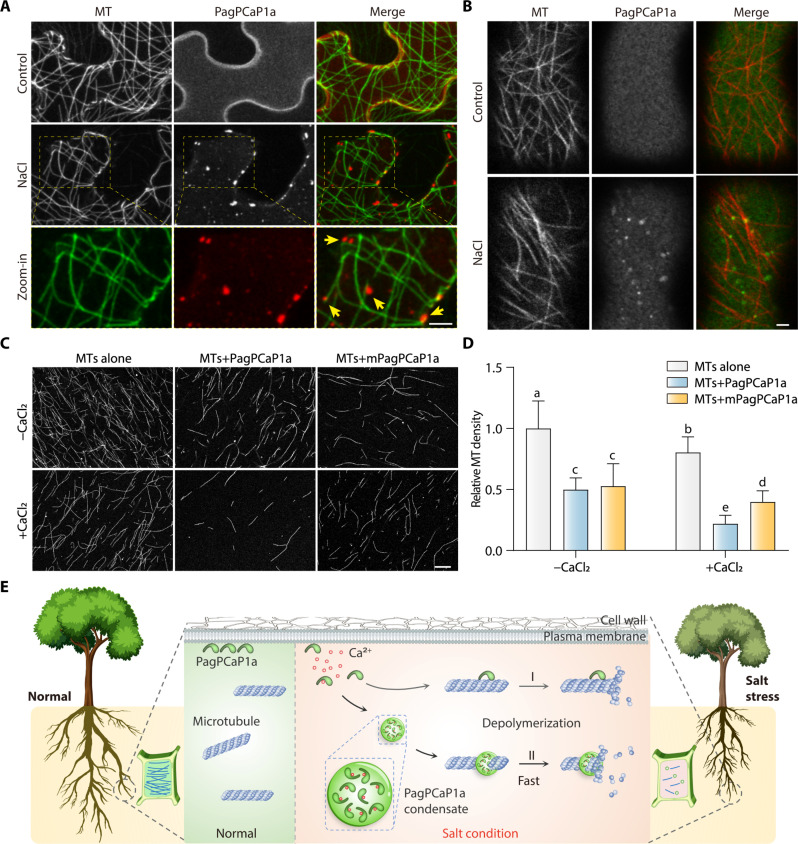
图6 PagPCaP1a凝聚物在盐胁迫下增强微管解聚的效率
本研究确定了杂交杨树幼苗的盐度胁迫反应机制。盐胁迫诱导PagPCaP1a表达和PagPCaP1a蛋白的相分离,以钙依赖性方式形成PagPCaP1a凝聚物。PagPCaP1a凝聚物的形成部分由蛋白质羧基末端的VEEEKK基序驱动,该基序在盐度胁迫下迅速解聚微管。
植物遗传转化又称植物基因工程,可利用重组DNA和细胞、组织培养等技术,改良植物性状,培育优质高产作物新品种。
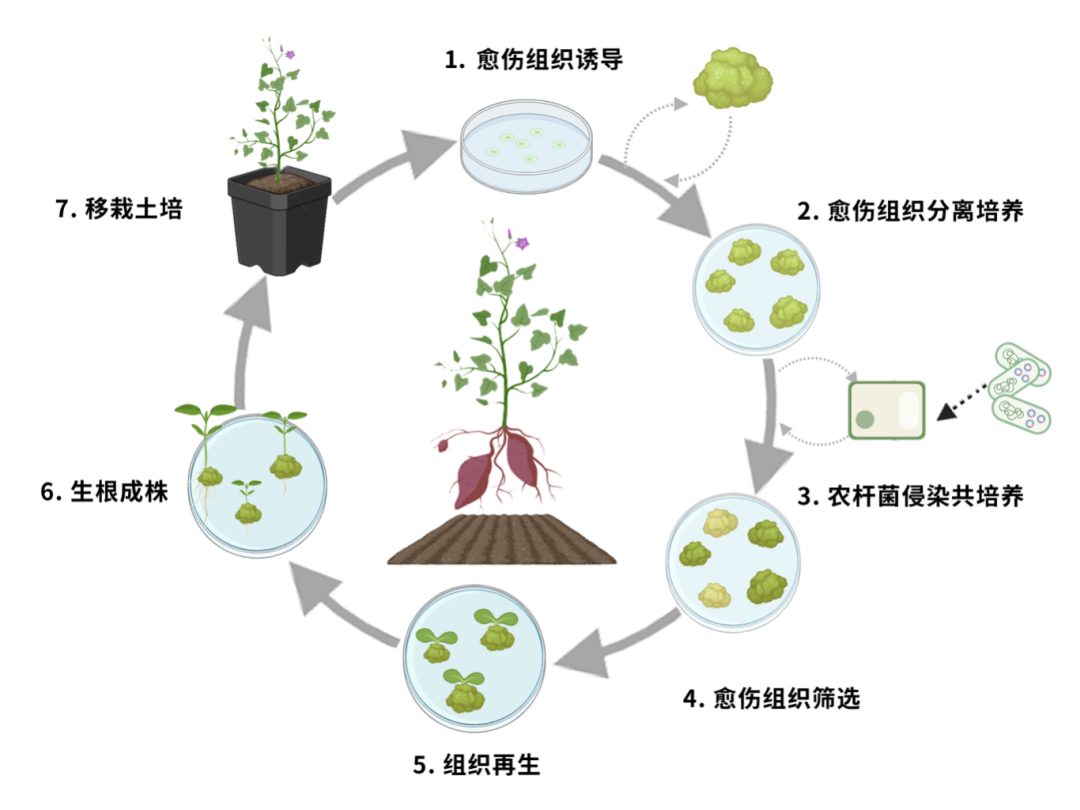
遗传转化技术流程
遗传转化手段可以为经过转录组、蛋白组、代谢组等多组学手段筛选出的目标基因或分子,提供直观、可靠的结论验证。
除了上面解读的文章外,还有很多优秀的高分文章采用相似策略,利用遗传转化获得的转基因植株进行研究。



部分相关文献
根据网络数据,分子育种相关国自然项目资助金额已达到18,411万元。
图源:网络
然而,作为一种发展成熟的技术,虽然转基因植株的构建效率、质量等环节对实验进度的影响重大,但也常常是比较容易被研究人员忽略的重点环节。
遗传转化的交付周期和成功率,哪个更重要?
此次遗传转化服务升级,我们承诺:晚交、少株必赔!
硬性交付指标无水分,保障您的每一次下单权益。
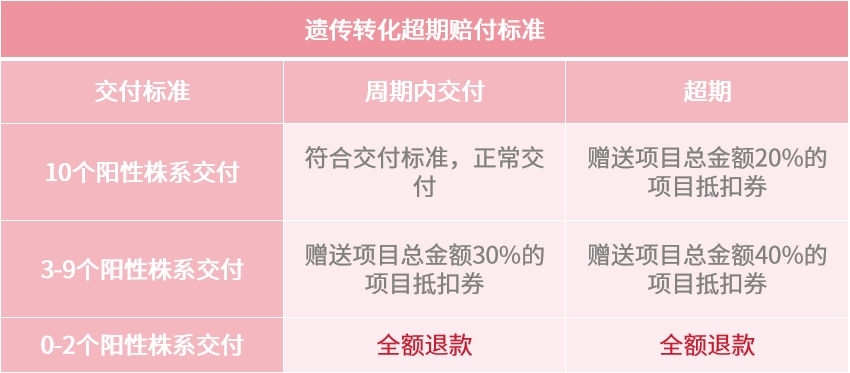
遗传转化项目超期赔付标准
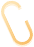
注:
遗传转化产品周期为范围,如3-5个月,超期指超出5个月。
产品周期范围为分子实验周期+遗传转化的周期。
赠送项目抵用券可用于三黍全部产品。
更多细节,欢迎咨询详细了解。
售中全流程透明化,您可以随时掌握监督项目情况!
项目流程图
作为一家深耕行业十年的公司,目前,三黍生物已拥有多个植物品种的稳定遗传转化体系,服务农科院、农业大学课题组、综合大学生命学院/农学院课题组等不同研究方向多位客户,成功发表多篇文章。
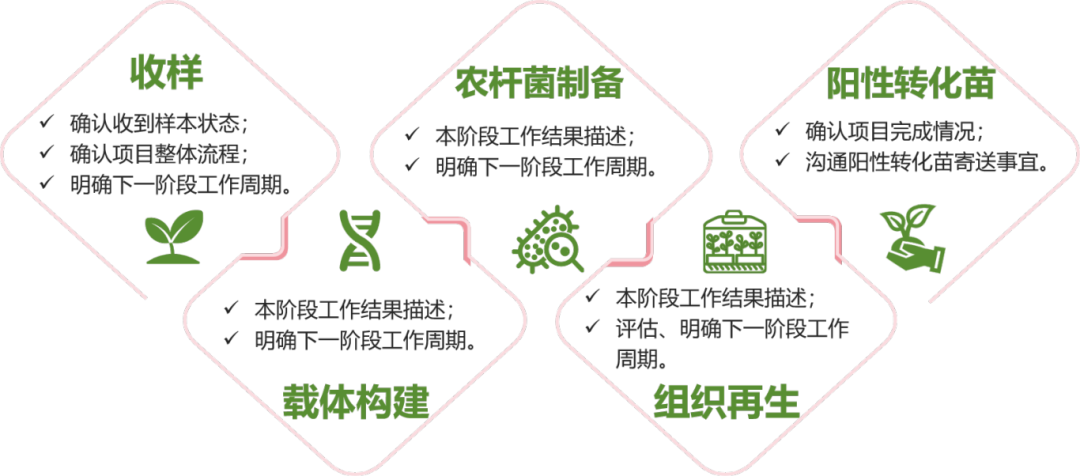
下列所有物种均适用于上述“0风险保障”条款,如果您有其他感兴趣的物种,也欢迎联系我们详细沟通!
三黍生物遗传转化部分物种
Q1:为什么转化周期那么长?
A:三黍的遗传转化属于稳转体系,防止因周期特别短的瞬转手段或非标准愈伤转化体系,导致出现基因表达不稳定、植株为嵌合体等情况,对您的项目进度造成不良影响。植物的自然生长过程较长,平均4-5个月的周期属于正常范围。
Q2:4个月一定能出阳性苗吗?
A:不同基因的转化效率、表达水平会因为植物的自身特性而有所差异。有些物种转化较容易,有些物种较难。部分基因转化效率不高,有些比较重要或功能冗余基因过表达后的表达量波动很大,因此需要视具体情况而定。我们会跟进转化进度,有问题及时和您沟通。
Q3:这么长的转化周期,这段时间我能做什么?
A:在等待遗传转化项目完成期间,各位老师可以根据自己的实验进度先安排在野生型中对目标基因的表达量、功能进行检测(介绍我们的检测服务),也可以根据目标基因功能选择做一些下游的转录组、蛋白组或代谢组分析,我们可以辅助进行课题挖掘和思路设计。
如果您还有其他问题,欢迎后台联系我们详细咨询!
滑动查看更多
高效率+高成功率
独家稳定技术,从基因克隆到植物再生
一站式解决方案!
活动中下单任意遗传转化项目,即可享受:
+500元,可额外享受一次专业载体构建服务;
+800元,可额外享受一次荧光定量PCR检测服务(含10个样本)。
前100名咨询客户
可获得
免费项目规划和技术咨询服务
根据您的具体需求提供个性化定制服务,让科研更加得心应手!
滑动查看更多:
排版:野凌
审核:三黍生物企宣部




